维百奥(北京)生物科技有限公司
8 年
手机商铺
- NaN
- 0.10000000000000009
- 0.10000000000000009
- 2.1
- 2.1
维百奥(北京)生物科技有限公司
入驻年限:8 年
- 联系人:
王经理
- 所在地区:
北京 大兴区
- 业务范围:
试剂、抗体、细胞库 / 细胞培养、技术服务、ELISA 试剂盒、耗材、实验室仪器 / 设备
- 经营模式:
代理商 经销商
推荐产品
公司新闻/正文
酶联免疫吸附测定(ELISA)技术详解:从原理到操作的核心要素
19 人阅读发布时间:2026-04-03 09:46
酶联免疫吸附测定(Enzyme-Linked Immunosorbent Assay,ELISA)是生命科学基础研究中最常用的蛋白定量技术之一,有灵敏度高、特异性良好和操作便捷性的优点,是实验室检测蛋白质、多肽、抗体及激素等生物分子的重要手段。
一、技术原理与核心组分
ELISA的技术基础建立在抗原-抗体特异性结合反应之上,通过酶催化底物显色实现目标分子的定量检测。整个检测体系包含几个核心组分:
固相载体是ELISA反应的基础平台,通常采用聚苯或聚氯材质的96孔微孔板。此类材料对蛋白质具有高亲和吸附能力,能够有效固定抗原或捕获抗体。
酶标记物是信号放大的关键元件,最常用的酶包括辣根过氧化物酶和碱性磷酸酶。辣根过氧化物酶与其底物四甲基胺反应时,可产生可溶性蓝色产物,加入酸性终止液后转变为黄色,在450nm波长处产生特征吸收峰。
洗涤系统通过磷酸盐缓冲液或专用洗涤缓冲液,在每一步反应后去除未结合的游离物质,有效降低背景信号。
二、主要检测模式
根据检测目标和实验设计的不同,ELISA可分为几种标准模式:
直接法是最简化的检测形式,将抗原直接包被于固相表面,加入酶标记的特异性抗体形成抗原-抗体复合物,最后通过底物显色进行检测。直接法操作步骤少、耗时短,适用于筛选性实验。
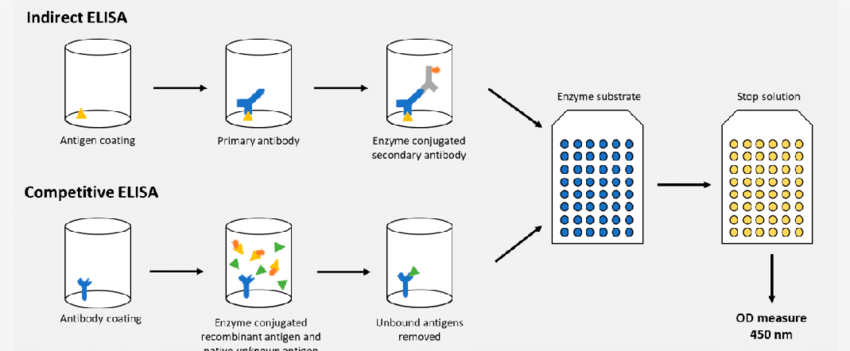
间接法在直接法基础上增加了未标记的一抗孵育步骤,随后使用酶标记的二抗进行信号放大。由于二抗可识别同一物种来源的一抗,间接法信号增强效果显著,且无需标记每种特异性抗体,在抗体效价测定中应用广泛。
夹心法采用成对抗体进行检测,首先将捕获抗体包被于固相表面,加入待测样本使抗原与捕获抗体结合,再加入酶标记的检测抗体形成“抗体-抗原-抗体”复合物。由于双重识别提高了特异性,夹心法尤其适用于大分子蛋白的定量检测。
竞争法基于标记抗原与样本抗原竞争结合有限抗体的原理,适合检测小分子激素或药物等无法同时结合两个抗体的分析物。竞争法的显色信号强度与样本中待测物浓度呈负相关。
三、关键操作要素
1. 样本前处理
样本质量直接影响检测结果的可靠性。血清样本应避免溶血,因血红蛋白释放的过氧化物酶会干扰显色反应;血浆样本需注意抗凝剂的选择,肝素钠和EDTA均可使用,但需确保充分混匀避免局部凝血。细胞培养上清样本建议离心去除细胞碎片,对于低浓度样本可考虑浓缩处理。
2. 加样操作规范
加样是ELISA操作中最重要的环节之一。建议使用校准合格的精密移液器,加样时枪头垂直插入孔底并避免接触孔壁,缓慢加入样品后轻弹板边混匀。不同样本之间必须更换枪头,防止交叉污染。对于大批量样本检测,应注意控制加样时间差,建议使用多通道移液器并保持各孔孵育时间一致。
3. 孵育条件控制
孵育温度和时间的精确控制对实验结果至关重要。通常采用37℃恒温孵育,反应板应水平放置并确保温度均匀,避免堆叠或靠近热源。对于过夜孵育,推荐在4℃条件下进行,可减少非特异性结合并提高灵敏度。孵育时需保持适当湿度,防止边缘孔液体蒸发导致的边缘效应。
4. 洗涤程序优化
洗涤步骤旨在去除未结合的游离物质,其彻底程度直接影响背景信号和检测特异性。手工洗涤时,每孔加满洗涤液后静置30-60秒再弃去,重复3-5次,最后在干净吸水纸上拍干。使用洗板机时需定期校准洗液体积和吸液残留量。过度洗涤可能导致结合的抗原-抗体复合物解离,造成信号偏低。
5. 显色与终止
底物溶液应现用现配,避免光照。加入底物后,酶促显色反应通常在室温避光条件下进行15-30分钟,待阳性对照孔显色达到预期强度时,立即加入终止液。终止液应快速、均匀加入所有反应孔,避免顺序加样导致的时间差影响。
6. 信号读取与数据处理
使用酶标仪在相应波长下读取吸光度值,常用检测波长为450nm,参比波长为570nm或630nm以校正背景干扰。标准曲线建议采用四参数逻辑斯蒂拟合,相关系数R²应大于0.99。待测样本浓度需根据标准曲线计算,并乘以相应稀释倍数。
四、质量控制与标准化
为确保ELISA检测结果的准确性和可重复性,实验过程中应设置必要的质控对照。例如需要设置空白对照用于校正系统背景,阴性对照验证试剂特异性,阳性对照正常则确认检测体系正常有效。标准品复孔检测并计算变异系数,批内变异系数应小于10%,批间变异系数小于15%。